Kovalente bindinger[]
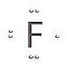
En kovalent binding er når atomerne danner fælles elektronpar.

Et eksempel kunne være difluor (F2). Når to fluor atomer binder sig sammen for at danne et difluormolekyle, går de sammen på den måde, at de sætter deres to uparrede elektroner sammen, så de uparrende elektroner tilsammen danner et fælles elektronpar.

Dette resulterer også i at hvert af atomerne har 8 elektroner omkring den yderste skal, de har altså opnået den samme elektron struktur som grundstoffet neon.
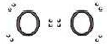
Et andet eksempel kunne være oxygen. Her går de igen sammen og deles om nogle atomer, men denne gang, da oxygen har 6 elektroner i yderste skal, deles de om 4 elektroner. Og derfor dannes der to fælles elektronpar, dette kaldes for en dobbeltbinding.
To atomer kan godt have flere fælles elektronpar. Det kaldes kovalente dobbeltbindinger eller trippelbindinger.
Set d. 20/1 2016 af lærer: Kirsten (KTL)